La enfermedad de células falciformes ha sido durante mucho tiempo una condición hereditaria devastadora que afecta desproporcionadamente a las comunidades del África subsahariana y la India. Durante décadas, los pacientes soportaron ciclos de crisis de dolor insoportables y agotamiento severo sin una verdadera cura a la vista. Ese panorama ha cambiado drásticamente. Después de años de meticulosa investigación genética, los científicos han desbloqueado un mecanismo para curar funcionalmente la enfermedad engañando al cuerpo para que produzca células sanguíneas sanas.
En reconocimiento a este descubrimiento transformador, el * * Premio Breakthrough en Ciencias de la Vida * * otorgó 3 3 millones al Dr. Swee Lay Thein y al Dr. Stuart Orkin. Su trabajo identificó un “interruptor” genético específico que, cuando se activa, permite que el cuerpo evite los genes defectuosos responsables de la anemia falciforme y la beta-talasemia.
La Clave Biológica: Despertar la Hemoglobina Fetal
Para comprender el avance, es esencial observar cómo se desarrolla la sangre humana. En el útero, los humanos producen * * hemoglobina fetal, una proteína altamente eficiente para extraer oxígeno de la circulación de la madre. Poco después del nacimiento, el cuerpo apaga naturalmente esta producción y cambia a hemoglobina adulta**.
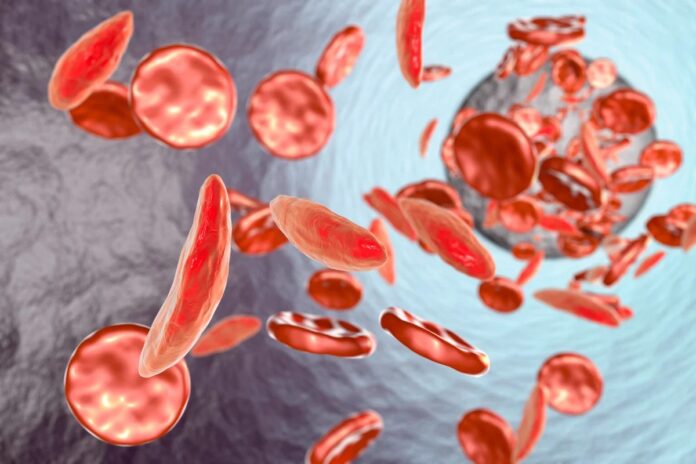
En individuos con anemia falciforme o beta-talasemia, la hemoglobina adulta tiene malformaciones o es deficiente, lo que produce los característicos glóbulos rojos en forma de hoz que obstruyen los vasos y causan dolor. Sin embargo, la hemoglobina fetal sigue siendo perfectamente capaz de transportar oxígeno durante toda la vida. El único obstáculo era que los científicos no sabían cómo mantener en funcionamiento la línea de producción fetal después del nacimiento.
El descubrimiento crítico fue la identificación de un gen llamado * * BCL11A**. Este gen actúa como un supresor, desactivando activamente la producción de hemoglobina fetal a medida que crecemos. Orkin y Thein se dieron cuenta de que si podían desactivar BCL11A, podrían convencer al cuerpo para que continúe produciendo hemoglobina fetal sana, neutralizando efectivamente los efectos de la enfermedad.
De la Observación Clínica al Descubrimiento Genético
El camino hacia este descubrimiento no fue una línea recta, sino el resultado de dos enfoques de investigación complementarios que abarcaron más de dos décadas.
** El enfoque del Dr. Thein: Siguiendo a las Familias
El trabajo del Dr. Thein comenzó con una pregunta clínica engañosamente simple: ¿Por qué algunos pacientes con beta-talasemia tienen síntomas notablemente leves, mientras que otros requieren transfusiones de por vida?
Notó que los pacientes con formas más leves de la enfermedad a menudo poseían niveles naturalmente altos de hemoglobina fetal. Para encontrar la causa genética, Thein viajó a Malawi, donde identificó a una familia numerosa y multigeneracional con casos inusualmente leves de la enfermedad. Al estudiar a 210 individuos a lo largo de siete generaciones, su equipo rastreó el rasgo hasta una región genética específica. Los estudios de asociación de todo el genoma finalmente identificaron a * * BCL11A** como el regulador responsable de esta variación, confirmándolo como un objetivo terapéutico viable.
** El enfoque del Dr. Orkin: Ingeniería de la Cura**
Mientras Thein identificó el gen en poblaciones humanas, Orkin se centró en demostrar que podía manipularse terapéuticamente. En 2011, su equipo diseñó ratones con anemia falciforme y utilizó herramientas genéticas para deshabilitar el gen BCL11A específicamente en sus glóbulos rojos en desarrollo. El resultado fue sorprendente: los ratones se corrigieron por completo y se mantuvieron sanos.
Esta prueba de concepto demostró que dirigirse a un solo gen era suficiente para resolver la enfermedad. La llegada de la tecnología de edición genética CRISPR poco después proporcionó la herramienta precisa necesaria para traducir este modelo de ratón en terapia humana.
Una Nueva Era de Tratamiento
El avance teórico ahora se ha convertido en una realidad clínica. En 2023, se aprobaron las primeras terapias de edición genética para la anemia falciforme: * * Casgevy * (de Vertex Pharmaceuticals y CRISPR Therapeutics) y * * Lyfgenia * (de bluebird bio / Genetix Biotherapeutics).
Los primeros resultados de los ensayos clínicos han sido transformadores.
* * * Cura funcional: * * Más del 90% de los participantes en el ensayo Vertex mostraron mejoría funcional.
* * * Resolución de los síntomas: * * Los pacientes con anemia falciforme informaron un cese completo de las crisis dolorosas.
* * * Independencia transfusional: * * Los pacientes con beta-talasemia ya no requerían transfusiones de sangre ni trasplantes de médula ósea.
“Antes, era una enfermedad miserable… Después de recibir tratamiento, tienen una nueva oportunidad de vida”, señaló el Dr. Orkin, destacando el profundo impacto en la capacidad de los pacientes para trabajar y vivir normalmente.
El Desafío de la Accesibilidad
A pesar del triunfo médico, persisten importantes barreras de acceso. Las terapias aprobadas actualmente son tratamientos * * ex vivo**, lo que significa que requieren:
1. Recolección de las células madre del paciente.
2. Editarlos en un laboratorio especializado.
3. Administrar quimioterapia intensiva para limpiar la médula ósea.
4. Reinfundir las celdas editadas.
Este proceso es físicamente agotador, logísticamente complejo y extraordinariamente costoso, con un costo de entre 2 2 millones y 3 3 millones por paciente. En consecuencia, estos tratamientos son actualmente inaccesibles para las poblaciones del África subsahariana y la India, que soportan la mayor carga de la enfermedad.
El Camino a Seguir: Hacia Curas Más Simples
Reconociendo estas limitaciones, la comunidad científica está girando hacia soluciones de próxima generación. Tanto el Dr. Thein como el Dr. Orkin ahora están enfocados en terapias de moléculas pequeñas, medicamentos que podrían tomarse como una píldora en lugar de requerir una edición genética compleja.
-
-
- El laboratorio de Orkin * * está investigando los mecanismos detallados del cambio de hemoglobina para desarrollar medicamentos que puedan revertir farmacológicamente al cuerpo a producir hemoglobina fetal.
-
-
-
- La investigación de Thein** se centra en moléculas pequeñas que pueden prevenir o abortar crisis de dolor severo, abordando una necesidad clínica inmediata e insatisfecha.
-
Si bien las terapias genéticas actuales ofrecen una cura poderosa para quienes pueden acceder a ellas, el objetivo final es desarrollar tratamientos asequibles y accesibles que puedan llegar a los pacientes de todo el mundo. El descubrimiento de BCL11A ha proporcionado el mapa; el siguiente paso es construir vehículos que puedan llevar esta cura a todos los rincones del mundo.
** Conclusión**
La identificación del gen BCL11A representa un salto monumental en el tratamiento de la anemia falciforme, pasando del manejo a la cura funcional. Si bien las terapias genéticas actuales son costosas y complejas, validan la vía científica, impulsando la investigación urgente hacia tratamientos basados en medicamentos más simples y accesibles para los millones que aún los necesitan.