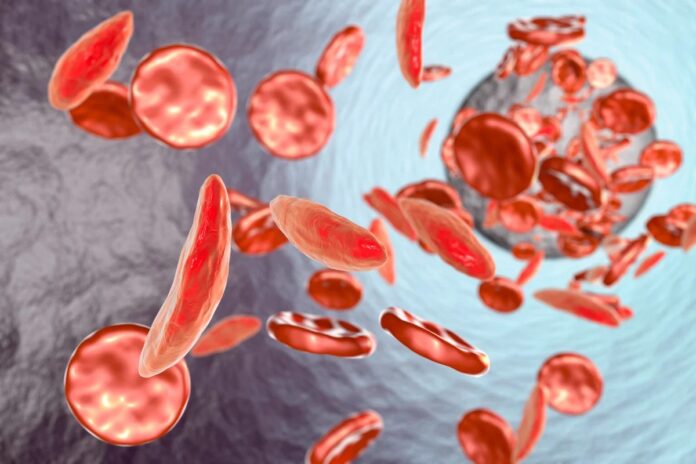
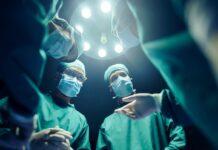
Серповидноклеточная анемия долгое время оставалась разрушительным наследственным заболеванием, непропорционально затрагивающим сообщества в странах к югу от Сахары и в Индии. Десятилетиями пациенты переносили циклы невыносимых болевых кризов и тяжелой усталости, не видя надежды на настоящее исцеление. Однако эта картина резко изменилась. После многих лет кропотливых генетических исследований ученым удалось раскрыть механизм, позволяющий функционально излечить болезнь, заставив организм производить здоровые клетки крови.
В знак признания этого трансформационного открытия Премия за прорыв в области наук о жизни присудила 3 миллиона долларов доктору Свэ Лэй Тейну и доктору Стюарту Оркину. Их работа выявила специфический генетический «выключатель», который, будучи активированным, позволяет организму обойти дефектные гены, ответственные за серповидноклеточную анемию и бета-талассемию.
Биологический ключ: пробуждение фетального гемоглобина
Чтобы понять суть прорыва, важно взглянуть на то, как развивается кровь у человека. В утробе матери люди производят фетальный гемоглобин — белок, высокоэффективный в извлечении кислорода из кровообращения матери. Сразу после рождения организм естественным образом прекращает его выработку и переключается на взрослый гемоглобин.
У людей с серповидноклеточной анемией или бета-талассемией взрослый гемоглобин либо деформирован, либо его недостаточно, что приводит к образованию характерных серповидных эритроцитов, закупоривающих сосуды и вызывающих боль. Однако фетальный гемоглобин остается полностью способным переносить кислород на протяжении всей жизни. Единственным препятствием было то, что ученые не знали, как сохранить линию производства фетального гемоглобина активной после рождения.
Критическим открытием стала идентификация гена BCL11A. Этот ген действует как супрессор, активно отключая производство фетального гемоглобина по мере нашего роста. Оркин и Тейн осознали, что если они смогут деактивировать BCL11A, они смогут подтолкнуть организм к продолжению выработки здорового фетального гемоглобина, эффективно нейтрализуя последствия заболевания.
От клинических наблюдений к генетическому открытию
Путь к этому открытию не был прямым, а стал результатом двух взаимодополняющих исследовательских подходов, охвативших более двух десятилетий.
Подход доктора Тейна: следование по семейным линиям
Работа доктора Тейна началась с обманчиво простого клинического вопроса: Почему у некоторых пациентов с бета-талассемией симптомы remarkably мягкие, в то время как другим требуются пожизненные переливания крови?
Он заметил, что пациенты с более легкими формами заболевания часто имели естественный высокий уровень фетального гемоглобина. Чтобы найти генетическую причину, Тейн отправился в Малави, где он выявил большую многопоколенческую семью с необычно легкими случаями заболевания. Изучив 210 человек на протяжении семи поколений, его команда проследила черту до конкретной генетической области. Исследования ассоциаций во всем геноме в конечном итоге указали на BCL11A как на регулятор, ответственный за эту вариацию, подтвердив его как жизнеспособную терапевтическую мишень.
Подход доктора Оркина: инженерия лечения
Пока Тейн идентифицировал ген в человеческих популяциях, Оркин сосредоточился на доказательстве того, что им можно манипулировать в терапевтических целях. В 2011 году его команда создала мышей с серповидноклеточной анемией и использовала генетические инструменты для отключения гена BCL11A конкретно в их развивающихся эритроцитах. Результат был поразительным: мыши были полностью исправлены и оставались здоровыми.
Это доказательство концепции продемонстрировало, что воздействия на один ген достаточно для решения проблемы заболевания. Появление технологии редактирования генов CRISPR вскоре после этого предоставило точный инструмент, необходимый для перевода этой мышиной модели в человеческую терапию.
Новая эра лечения
Теоретический прорыв стал клинической реальностью. В 2023 году были одобрены первые терапии на основе редактирования генов для серповидноклеточной анемии: Casgevy (от Vertex Pharmaceuticals и CRISPR Therapeutics) и Lyfgenia (от bluebird bio/Genetix Biotherapeutics).
Ранние результаты клинических испытаний оказались трансформационными.
* Функциональное излечение: Более 90% участников испытания Vertex показали функциональное улучшение.
* Решение симптомов: Пациенты с серповидноклеточной анемией сообщили о полном прекращении болевых кризов.
* Независимость от переливаний: Пациенты с бета-талассемией больше не нуждались в переливаниях крови или трансплантации костного мозга.
«Раньше это было miserable заболевание… После лечения они получают новую жизнь», — отметил доктор Оркин, подчеркивая глубокое влияние на способность пациентов работать и жить нормально.
Проблема доступности
Несмотря на медицинский триумф, остаются значительные барьеры в отношении доступа. Текущие одобренные терапии являются ex vivo лечениями, что означает, что они требуют:
1. Забора стволовых клеток пациента.
2. Их редактирования в специализированной лаборатории.
3. Проведения интенсивной химиотерапии для очистки костного мозга.
4. Реинфузии отредактированных клеток.
Этот процесс физически изнурителен, логистически сложен и необычайно дорог, обходясь от 2 до 3 миллионов долларов на пациента. В результате эти методы лечения в настоящее время недоступны для населения в странах к югу от Сахары и в Индии, которые несут наибольшее бремя заболевания.
Дорога вперед: к более простым методам лечения
Признавая эти ограничения, научное сообщество переключается на решения следующего поколения. Оба доктора, Тейн и Оркин, теперь сосредоточены на терапии малыми молекулами — лекарствах, которые можно принимать в виде таблетки, а не требующих сложного редактирования генов.
- Лаборатория Оркина исследует подробные механизмы переключения гемоглобина для разработки препаратов, которые могут фармакологически вернуть организм к выработке фетального гемоглобина.
- Исследования Тейна сосредоточены на малых молекулах, которые могут предотвращать или прерывать тяжелые болевые кризы, решая немедленную и неудовлетворенную клиническую потребность.
Хотя текущие генные терапии предлагают мощное лечение для тех, кто имеет к ним доступ, конечная цель — разработать доступные и доступные методы лечения, которые могут достичь пациентов по всему миру. Открытие BCL11A предоставило карту; следующий шаг — создание транспортных средств, которые смогут доставить это лекарство в каждый уголок планеты.
Заключение
Идентификация гена BCL11A представляет собой грандиозный скачок в лечении серповидноклеточной анемии, переход от управления симптомами к функциональному излечению. Хотя текущие генные терапии дороги и сложны, они подтверждают научный путь, стимулируя срочные исследования в сторону более простых и доступных лекарственных методов лечения для миллионов нуждающихся.