La drépanocytose est depuis longtemps une maladie héréditaire dévastatrice, affectant de manière disproportionnée les communautés d’Afrique subsaharienne et d’Inde. Pendant des décennies, les patients ont enduré des cycles de crises douloureuses atroces et d’épuisement sévère sans véritable remède en vue. Ce paysage a radicalement changé. Après des années de recherches génétiques méticuleuses, les scientifiques ont mis au point un mécanisme permettant de guérir fonctionnellement la maladie en incitant le corps à produire des cellules sanguines saines.
En reconnaissance de cette découverte transformatrice, le Breakthrough Prize in Life Sciences a décerné 3 millions de dollars au Dr Swee Lay Thein et au Dr Stuart Orkin. Leurs travaux ont identifié un “commutateur” génétique spécifique qui, lorsqu’il est inversé, permet au corps de contourner les gènes défectueux responsables de la drépanocytose et de la bêta-thalassémie.
La Clé Biologique: Réveiller l’Hémoglobine Fœtale
Pour comprendre la percée, il est essentiel de regarder comment le sang humain se développe. Dans l’utérus, les humains produisent de l’hémoglobine fœtale, une protéine très efficace pour extraire l’oxygène de la circulation de la mère. Peu de temps après la naissance, le corps arrête naturellement cette production et passe à l’hémoglobine adulte.
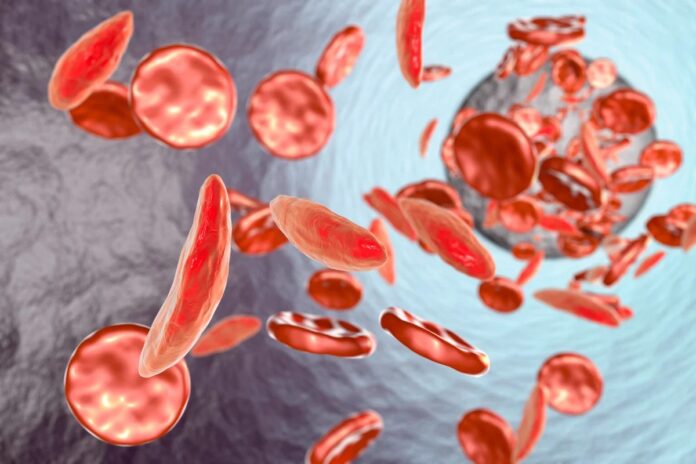
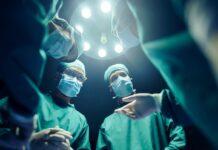
Chez les personnes atteintes de drépanocytose ou de bêta-thalassémie, l’hémoglobine adulte est soit mal formée, soit déficiente, ce qui conduit aux globules rouges caractéristiques en forme de faucille qui obstruent les vaisseaux et provoquent des douleurs. Cependant, l’hémoglobine fœtale reste parfaitement capable de transporter de l’oxygène tout au long de la vie. Le seul obstacle était que les scientifiques ne savaient pas comment faire fonctionner la chaîne de production fœtale après la naissance.
La découverte critique a été l’identification d’un gène appelé BCL11A. Ce gène agit comme un suppresseur, désactivant activement la production d’hémoglobine fœtale à mesure que nous grandissons. Orkin et Thein ont réalisé que s’ils pouvaient désactiver BCL11A, ils pourraient inciter le corps à continuer à produire de l’hémoglobine fœtale saine, neutralisant efficacement les effets de la maladie.
De l’Observation Clinique à la Découverte Génétique
Le chemin vers cette découverte n’était pas une ligne droite, mais le résultat de deux approches de recherche complémentaires s’étendant sur plus de deux décennies.
** L’approche du Dr Thein: Suivre les familles
Le travail du Dr Thein a commencé par une question clinique d’une simplicité trompeuse: Pourquoi certains patients atteints de bêta-thalassémie présentent-ils des symptômes remarquablement légers alors que d’autres nécessitent des transfusions à vie?
Il a remarqué que les patients atteints de formes plus bénignes de la maladie possédaient souvent des taux naturellement élevés d’hémoglobine fœtale. Pour trouver la cause génétique, Thein s’est rendu au Malawi, où il a identifié une grande famille multigénérationnelle avec des cas inhabituellement bénins de la maladie. En étudiant 210 individus sur sept générations, son équipe a retracé le trait à une région génétique spécifique. Des études d’association à l’échelle du génome ont finalement identifié BCL11A comme régulateur responsable de cette variation, la confirmant comme une cible thérapeutique viable.
** L’approche du Dr Orkin: Concevoir le remède**
Alors que Thein a identifié le gène dans les populations humaines, Orkin s’est concentré sur la preuve qu’il pouvait être manipulé thérapeutiquement. En 2011, son équipe a conçu des souris atteintes d’anémie falciforme et a utilisé des outils génétiques pour désactiver le gène BCL11A spécifiquement dans leurs globules rouges en développement. Le résultat a été frappant: les souris ont été complètement corrigées et sont restées en bonne santé.
Cette preuve de concept a démontré que le ciblage d’un seul gène était suffisant pour résoudre la maladie. L’arrivée de la technologie d’édition de gènes CRISPR peu de temps après a fourni l’outil précis nécessaire pour traduire ce modèle murin en thérapie humaine.
Une Nouvelle Ère de Traitement
La percée théorique est maintenant devenue une réalité clinique. En 2023, les premières thérapies d’édition de gènes pour la drépanocytose ont été approuvées: * * Casgevy (par Vertex Pharmaceuticals et CRISPR Therapeutics) et * * Lyfgenia (par bluebird bio / Genetix Biotherapeutics).
Les premiers résultats des essais cliniques ont été transformateurs.
* * * Guérison fonctionnelle: * * Plus de 90% des participants à l’essai Vertex ont montré une amélioration fonctionnelle.
* * * Résolution des symptômes: * * Les patients atteints de drépanocytose ont signalé un arrêt complet des crises douloureuses.
* * * Indépendance transfusionnelle:* * Les patients atteints de bêta-thalassémie n’ont plus besoin de transfusions sanguines ni de greffes de moelle osseuse.
“Avant, c’était une maladie misérable… Une fois traités, ils ont un nouveau souffle sur la vie”, a noté le Dr Orkin, soulignant l’impact profond sur la capacité des patients à travailler et à vivre normalement.
Le Défi de l’Accessibilité
Malgré le triomphe médical, des obstacles importants subsistent en ce qui concerne l’accès. Les thérapies actuellement approuvées sont des traitements * * ex vivo**, ce qui signifie qu’elles nécessitent:
1. Récolter les cellules souches du patient.
2. Les éditer dans un laboratoire spécialisé.
3. Administration d’une chimiothérapie intensive pour nettoyer la moelle osseuse.
4. Réinjection des cellules éditées.
Ce processus est physiquement épuisant, logistiquement complexe et extraordinairement coûteux, coûtant entre 2 et 3 millions de dollars par patient. Par conséquent, ces traitements sont actuellement inaccessibles aux populations d’Afrique subsaharienne et d’Inde qui supportent le fardeau le plus lourd de la maladie.
La Route à Suivre: Vers Des Remèdes Plus Simples
Reconnaissant ces limites, la communauté scientifique s’oriente vers des solutions de nouvelle génération. Le Dr Thein et le Dr Orkin se concentrent maintenant sur * * les thérapies à petites molécules * * – des médicaments qui pourraient être pris sous forme de pilule plutôt que de nécessiter une édition complexe des gènes.
-
-
- Le laboratoire d’Orkin * * étudie les mécanismes détaillés du changement d’hémoglobine pour développer des médicaments qui peuvent ramener pharmacologiquement le corps à la production d’hémoglobine fœtale.
-
-
-
- La recherche de Thein* * est centrée sur les petites molécules qui peuvent prévenir ou interrompre les crises douloureuses sévères, répondant à un besoin clinique immédiat et non satisfait.
-
Alors que les thérapies géniques actuelles offrent un remède puissant à ceux qui peuvent y accéder, l’objectif ultime est de développer des traitements abordables et accessibles pouvant atteindre les patients du monde entier. La découverte de BCL11A a fourni la carte; la prochaine étape consiste à construire des véhicules capables de transporter ce remède aux quatre coins du monde.
** Conclusion**
L’identification du gène BCL11A représente un bond monumental dans le traitement de la drépanocytose, passant de la prise en charge à la guérison fonctionnelle. Bien que les thérapies géniques actuelles soient coûteuses et complexes, elles valident la voie scientifique, conduisant des recherches urgentes vers des traitements médicamenteux plus simples et plus accessibles pour les millions de personnes qui en ont encore besoin.