The Breakthrough 3 Million Breakthrough: come gli scienziati hanno decifrato il codice per curare l’anemia falciforme
L’anemia falciforme è stata a lungo una condizione ereditaria devastante, che colpisce in modo sproporzionato le comunità dell’Africa sub-sahariana e dell’India. Per decenni, i pazienti hanno sopportato cicli di crisi dolorose lancinanti e grave esaurimento senza una vera cura in vista. Quel paesaggio si è spostato drammaticamente. Dopo anni di meticolosa ricerca genetica, gli scienziati hanno sbloccato un meccanismo per curare funzionalmente la malattia ingannando il corpo nella produzione di cellule del sangue sane.
In riconoscimento di questa scoperta trasformativa, il Breakthrough Prize in Life Sciences ha assegnato 3 3 milioni al Dr. Swee Lay Thein e al Dr. Stuart Orkin. Il loro lavoro ha identificato uno specifico “interruttore” genetico che, quando capovolto, consente al corpo di bypassare i geni difettosi responsabili dell’anemia falciforme e della beta-talassemia.
La chiave biologica: risvegliare l’emoglobina fetale
Per capire la svolta, è essenziale guardare a come si sviluppa il sangue umano. Nell’utero, gli esseri umani producono * * emoglobina fetale**, una proteina altamente efficiente nell’estrarre ossigeno dalla circolazione della madre. Poco dopo la nascita, il corpo interrompe naturalmente questa produzione e passa all’emoglobina adulta.
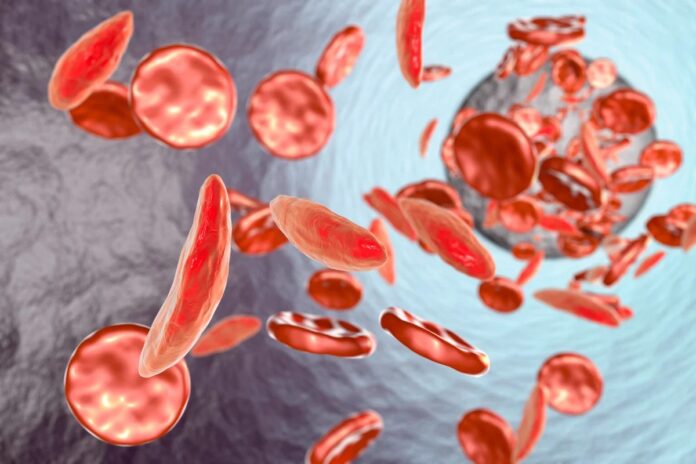
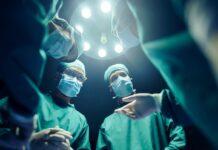
Negli individui con anemia falciforme o beta-talassemia, l’emoglobina adulta è malformata o carente, portando ai caratteristici globuli rossi a forma di falce che ostruiscono i vasi e causano dolore. Tuttavia, l’emoglobina fetale rimane perfettamente in grado di trasportare ossigeno per tutta la vita. L’unico ostacolo era che gli scienziati non sapevano come mantenere la linea di produzione fetale in esecuzione dopo la nascita.
La scoperta critica è stata l’identificazione di un gene chiamato * * BCL11A**. Questo gene agisce come soppressore, disattivando attivamente la produzione di emoglobina fetale man mano che cresciamo. Orkin e Thein si resero conto che se potevano disattivare BCL11A, potevano convincere il corpo a continuare a produrre emoglobina fetale sana, neutralizzando efficacemente gli effetti della malattia.
Dall’osservazione clinica alla scoperta genetica
Il percorso verso questa scoperta non era una linea retta, ma il risultato di due approcci di ricerca complementari che coprono oltre due decenni.
** L’approccio del Dr. Thein: seguire le famiglie
Il lavoro del Dr. Thein è iniziato con una domanda clinica apparentemente semplice: Perché alcuni pazienti con beta-talassemia hanno sintomi notevolmente lievi mentre altri richiedono trasfusioni per tutta la vita?
Ha notato che i pazienti con forme più lievi della malattia spesso possedevano naturalmente alti livelli di emoglobina fetale. Per trovare la causa genetica, Thein si è recato in Malawi, dove ha identificato una grande famiglia multi-generazionale con casi insolitamente lievi della malattia. Studiando 210 individui in sette generazioni, il suo team ha rintracciato il tratto in una specifica regione genetica. Studi di associazione Genome-wide alla fine individuato BCL11A come il regolatore responsabile di questa variazione, confermando come un bersaglio terapeutico praticabile.
L’approccio del Dr. Orkin: ingegnerizzare la cura *
Mentre Thein ha identificato il gene nelle popolazioni umane, Orkin si è concentrato sulla prova che potrebbe essere manipolato terapeuticamente. Nel 2011, il suo team ha ingegnerizzato topi con anemia falciforme e ha utilizzato strumenti genetici per disabilitare il gene BCL11A specificamente nei loro globuli rossi in via di sviluppo. Il risultato è stato sorprendente: i topi sono stati completamente corretti e sono rimasti sani.
Questo proof-of-concept ha dimostrato che il targeting di un singolo gene era sufficiente per risolvere la malattia. L’arrivo della tecnologia di editing genetico CRISPR poco dopo ha fornito lo strumento preciso necessario per tradurre questo modello murino in terapia umana.
Una nuova era di trattamento
La svolta teorica è ora diventata realtà clinica. Nel 2023 sono state approvate le prime terapie di modifica genica per l’anemia falciforme: * * Casgevy * * (da Vertex Pharmaceuticals e CRISPR Therapeutics) e Lyfgenia (da bluebird bio/Genetix Biotherapeutics).
I primi risultati degli studi clinici sono stati trasformativi.
* * * Cura funzionale: * * Oltre il 90% dei partecipanti allo studio Vertex ha mostrato un miglioramento funzionale.
* * * Risoluzione dei sintomi: * * I pazienti con anemia falciforme hanno riportato una completa cessazione delle crisi dolorose.
* * * Indipendenza trasfusionale: * * I pazienti con beta-talassemia non hanno più bisogno di trasfusioni di sangue o trapianti di midollo osseo.
“Prima era una malattia miserabile… Dopo essere stati trattati, hanno una nuova prospettiva di vita”, ha osservato il dottor Orkin, evidenziando il profondo impatto sulla capacità dei pazienti di lavorare e vivere normalmente.
La sfida dell’accessibilità
Nonostante il trionfo medico, rimangono barriere significative per quanto riguarda l’accesso. Le attuali terapie approvate sono trattamenti ex vivo, il che significa che richiedono:
1. Raccolta delle cellule staminali del paziente.
2. Modificarli in un laboratorio specializzato.
3. Somministrazione di chemioterapia intensiva per eliminare il midollo osseo.
4. Reinfusione delle celle modificate.
Questo processo è fisicamente estenuante, logisticamente complesso e straordinariamente costoso, che costa tra $2 milioni e $3 milioni per paziente. Di conseguenza, questi trattamenti sono attualmente inaccessibili alle popolazioni dell’Africa sub-sahariana e dell’India che sopportano il più alto carico della malattia.
La strada da percorrere: verso cure più semplici
Riconoscendo questi limiti, la comunità scientifica si sta orientando verso soluzioni di prossima generazione. Sia il Dott. Thein che il Dott. Orkin ora sono messi a fuoco sulle piccole terapie della molecola-droghe che potrebbero essere prese come pillola piuttosto che richiedere l’editing genetico complesso.
-
-
- Il laboratorio di Orkin * * sta studiando i meccanismi dettagliati dell’interruttore dell’emoglobina per sviluppare farmaci che possono riportare farmacologicamente il corpo alla produzione di emoglobina fetale.
-
-
-
- La ricerca di Thein * * è centrata su piccole molecole che possono prevenire o abortire gravi crisi di dolore, affrontando un bisogno clinico immediato e insoddisfatto.
-
Mentre le attuali terapie geniche offrono una cura potente per coloro che possono accedervi, l’obiettivo finale è quello di sviluppare trattamenti accessibili e accessibili che possano raggiungere i pazienti a livello globale. La scoperta di BCL11A ha fornito la mappa; il passo successivo è la costruzione di veicoli in grado di trasportare questa cura in ogni angolo del mondo.
Conclusione
L’identificazione del gene BCL11A rappresenta un salto monumentale nel trattamento dell’anemia falciforme, passando dalla gestione alla cura funzionale. Mentre le attuali terapie geniche sono costose e complesse, convalidano il percorso scientifico, guidando la ricerca urgente verso trattamenti farmacologici più semplici e più accessibili per i milioni di persone ancora bisognose.