Sichelzellenkrankheit ist seit langem eine verheerende Erbkrankheit, von der Gemeinden in Afrika südlich der Sahara und Indien überproportional betroffen sind. Jahrzehntelang ertrugen die Patienten Zyklen qualvoller Schmerzkrisen und schwerer Erschöpfung, ohne dass eine echte Heilung in Sicht war. Diese Landschaft hat sich dramatisch verändert. Nach Jahren akribischer genetischer Forschung haben Wissenschaftler einen Mechanismus zur funktionellen Heilung der Krankheit freigeschaltet, indem sie den Körper dazu bringen, gesunde Blutzellen zu produzieren.
In Anerkennung dieser bahnbrechenden Entdeckung verlieh der ** Breakthrough Prize in Life Sciences ** Dr. Swee Lay Thein und Dr. Stuart Orkin 3 Millionen US-Dollar. Ihre Arbeit identifizierte einen spezifischen genetischen “Schalter”, der es dem Körper ermöglicht, die defekten Gene zu umgehen, die für Sichelzellenerkrankungen und Beta-Thalassämie verantwortlich sind.
Der biologische Schlüssel: Wiedererweckung des fetalen Hämoglobins
Um den Durchbruch zu verstehen, ist es wichtig zu untersuchen, wie sich menschliches Blut entwickelt. Im Mutterleib produziert der Mensch ** fötales Hämoglobin **, ein Protein, das hocheffizient Sauerstoff aus dem Kreislauf der Mutter extrahiert. Kurz nach der Geburt schaltet der Körper diese Produktion auf natürliche Weise ab und schaltet auf ** erwachsenes Hämoglobin ** um.
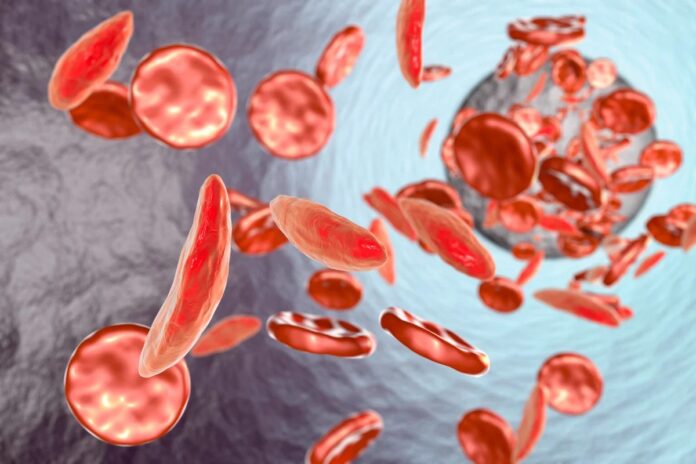
Bei Personen mit Sichelzellenanämie oder Beta-Thalassämie ist adultes Hämoglobin entweder missgebildet oder mangelhaft, was zu den charakteristischen sichelförmigen roten Blutkörperchen führt, die Gefäße verstopfen und Schmerzen verursachen. Fötales Hämoglobin bleibt jedoch während des gesamten Lebens vollkommen in der Lage, Sauerstoff zu transportieren. Die einzige Hürde war, dass die Wissenschaftler nicht wussten, wie sie die fetale Produktionslinie nach der Geburt am Laufen halten sollten.
Die entscheidende Entdeckung war die Identifizierung eines Gens namens ** BCL11A **. Dieses Gen wirkt als Suppressor und schaltet die Produktion von fötalem Hämoglobin aktiv aus, während wir wachsen. Orkin und Thein erkannten, dass sie, wenn sie BCL11A deaktivieren könnten, den Körper dazu bringen könnten, weiterhin gesundes fötales Hämoglobin zu produzieren, wodurch die Auswirkungen der Krankheit effektiv neutralisiert würden.
Von der klinischen Beobachtung zur genetischen Entdeckung
Der Weg zu dieser Entdeckung verlief nicht geradlinig, sondern war das Ergebnis zweier komplementärer Forschungsansätze, die sich über zwei Jahrzehnte erstreckten.
Dr. Theins Ansatz: Den Familien folgen
Dr. Theins Arbeit begann mit einer täuschend einfachen klinischen Frage: * Warum haben einige Patienten mit Beta-Thalassämie bemerkenswert milde Symptome, während andere lebenslange Transfusionen benötigen?*
Er bemerkte, dass Patienten mit milderen Formen der Krankheit oft von Natur aus einen hohen Gehalt an fötalem Hämoglobin aufwiesen. Um die genetische Ursache zu finden, reiste Thein nach Malawi, wo er eine große Familie mit mehreren Generationen mit ungewöhnlich leichten Krankheitsfällen identifizierte. Durch die Untersuchung von 210 Individuen über sieben Generationen hinweg verfolgte sein Team das Merkmal auf eine bestimmte genetische Region. Genomweite Assoziationsstudien identifizierten schließlich ** BCL11A ** als den für diese Variation verantwortlichen Regulator und bestätigten ihn als lebensfähiges therapeutisches Ziel.
** Dr. Orkins Ansatz: Entwicklung der Heilung**
Während Thein das Gen in menschlichen Populationen identifizierte, konzentrierte sich Orkin darauf zu beweisen, dass es therapeutisch manipuliert werden könnte. Im Jahr 2011 entwickelte sein Team Mäuse mit Sichelzellenanämie und verwendete genetische Werkzeuge, um das BCL11A-Gen spezifisch in ihren sich entwickelnden roten Blutkörperchen zu deaktivieren. Das Ergebnis war verblüffend: Die Mäuse waren vollständig korrigiert und blieben gesund.
Dieser Proof-of-Concept zeigte, dass die Ausrichtung auf ein einzelnes Gen ausreichte, um die Krankheit zu lösen. Die Einführung der CRISPR-Geneditierungstechnologie kurz darauf lieferte das präzise Werkzeug, das benötigt wurde, um dieses Mausmodell in die Humantherapie zu übersetzen.
Eine neue Ära der Behandlung
Der theoretische Durchbruch ist nun klinische Realität geworden. Im Jahr 2023 wurden die ersten geneditierenden Therapien für Sichelzellenerkrankungen zugelassen: ** Casgevy ** (von Vertex Pharmaceuticals und CRISPR Therapeutics) und ** Lyfgenia ** (von Bluebird bio / Genetix Biotherapeutics).
Frühe Ergebnisse aus klinischen Studien waren transformativ.
* ** Funktionelle Heilung: ** Mehr als 90% der Teilnehmer der Vertex-Studie zeigten eine funktionelle Verbesserung.
* ** Symptomauflösung: ** Patienten mit Sichelzellenanämie berichteten von einer vollständigen Beendigung schmerzhafter Krisen.
* ** Transfusionsunabhängigkeit: ** Patienten mit Beta-Thalassämie benötigten keine Bluttransfusionen oder Knochenmarktransplantationen mehr.
“Vorher war es eine erbärmliche Krankheit… Nachdem sie behandelt wurden, haben sie ein neues Leben “, bemerkte Dr. Orkin und hob die tiefgreifenden Auswirkungen auf die Fähigkeit der Patienten hervor, normal zu arbeiten und zu leben.
Die Herausforderung der Barrierefreiheit
Trotz des medizinischen Triumphs bestehen nach wie vor erhebliche Zugangsbarrieren. Derzeit zugelassene Therapien sind ** ex vivo ** Behandlungen, dh sie erfordern:
1. Gewinnung der Stammzellen des Patienten.
2. Bearbeitung in einem spezialisierten Labor.
3. Verabreichung einer intensiven Chemotherapie zur Reinigung des Knochenmarks.
4. Reinfusion der bearbeiteten Zellen.
Dieser Prozess ist körperlich anstrengend, logistisch komplex und außerordentlich teuer und kostet zwischen ** 2 Millionen und 3 Millionen US-Dollar pro Patient **. Folglich sind diese Behandlungen derzeit für die Bevölkerungsgruppen in Afrika südlich der Sahara und Indien, die die höchste Krankheitslast tragen, nicht zugänglich.
Der Weg in die Zukunft: Zu einfacheren Heilmitteln
Angesichts dieser Einschränkungen orientiert sich die wissenschaftliche Gemeinschaft an Lösungen der nächsten Generation. Sowohl Dr. Thein als auch Dr. Orkin konzentrieren sich jetzt auf ** niedermolekulare Therapien ** — Medikamente, die als Pille eingenommen werden könnten, anstatt eine komplexe Genbearbeitung zu erfordern.
- ** Orkins Labor ** untersucht die detaillierten Mechanismen des Hämoglobinwechsels, um Medikamente zu entwickeln, die den Körper pharmakologisch dazu bringen können, fötales Hämoglobin zu produzieren.
- ** Theins Forschung ** konzentriert sich auf kleine Moleküle, die schwere Schmerzkrisen verhindern oder abbrechen können und einen unmittelbaren und ungedeckten klinischen Bedarf adressieren.
Während aktuelle Gentherapien eine wirksame Heilung für diejenigen bieten, die Zugang zu ihnen haben, besteht das ultimative Ziel darin, erschwingliche, zugängliche Behandlungen zu entwickeln, die Patienten weltweit erreichen können. Die Entdeckung von BCL11A hat die Karte geliefert; Der nächste Schritt ist der Bau von Fahrzeugen, die dieses Heilmittel in jeden Winkel der Welt transportieren können.
Schlussfolgerung
Die Identifizierung des BCL11A-Gens stellt einen monumentalen Sprung in der Behandlung von Sichelzellenerkrankungen dar, der vom Management zur funktionellen Heilung übergeht. Während aktuelle Gentherapien teuer und komplex sind, validieren sie den wissenschaftlichen Weg und treiben die dringende Forschung in Richtung einfacherer, zugänglicherer arzneimittelbasierter Behandlungen für die Millionen, die noch immer bedürftig sind, voran.