De doorbraak van $ 3 miljoen: hoe wetenschappers de Code hebben gekraakt om sikkelcelziekte te genezen
Sikkelcelziekte is al lang een verwoestende erfelijke aandoening, die onevenredig veel gevolgen heeft voor gemeenschappen in Afrika ten zuiden van de Sahara en India. Tientallen jaren lang ondergingen patiënten cycli van ondraaglijke pijncrises en ernstige uitputting zonder dat er een echte remedie in zicht was. Dat landschap is dramatisch veranderd. Na jaren van nauwgezet genetisch onderzoek hebben wetenschappers een mechanisme ontsloten om de ziekte functioneel te genezen door het lichaam te misleiden om gezonde bloedcellen te produceren.
Als erkenning voor deze transformatieve ontdekking, heeft de** Breakthrough Prize In Life Sciences * * $3 miljoen toegekend aan Dr.Swee Lay Thein en Dr. Stuart Orkin. Hun werk identificeerde een specifieke genetische “schakelaar” die, wanneer omgedraaid, het lichaam in staat stelt de defecte genen te omzeilen die verantwoordelijk zijn voor sikkelcelziekte en bèta-thalassemie.
De Biologische Sleutel: Het Ontwaken Van Foetaal Hemoglobine
Om de doorbraak te begrijpen, is het essentieel om te kijken naar hoe menselijk bloed zich ontwikkelt. In de baarmoeder produceren mensen foetaal hemoglobine, een eiwit dat zeer efficiënt is in het extraheren van zuurstof uit de bloedsomloop van de moeder. Kort na de geboorte stopt het lichaam van nature deze productie en schakelt over naar volwassen hemoglobine.
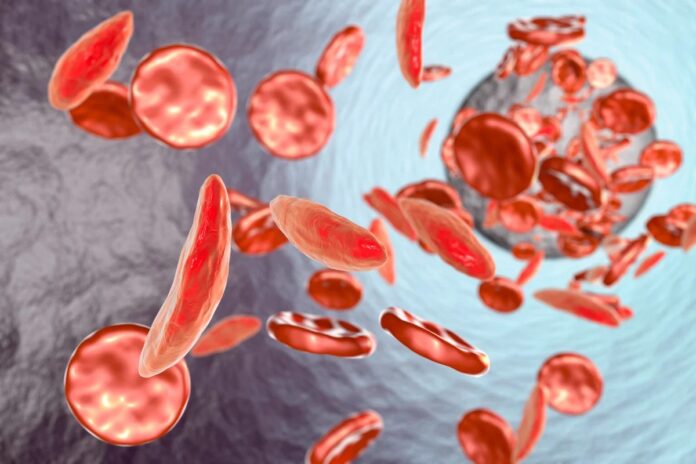
Bij personen met sikkelcelziekte of bèta-thalassemie is volwassen hemoglobine ofwel misvormd of tekort, wat leidt tot de karakteristieke sikkelvormige rode bloedcellen die bloedvaten verstoppen en pijn veroorzaken. Foetale hemoglobine blijft echter gedurende het hele leven perfect in staat zuurstof te vervoeren. De enige hindernis was dat wetenschappers niet wisten hoe ze de foetale productielijn na de geboorte konden laten draaien.
De kritische ontdekking was de identificatie van een gen genaamd BCL11A. Dit gen werkt als een onderdrukker, actief uitschakelen foetale hemoglobineproductie als we groeien. Orkin en Thein realiseerden zich dat als ze BCL11A konden deactiveren, ze het lichaam konden overhalen om gezond foetaal hemoglobine te blijven produceren, waardoor de effecten van de ziekte effectief werden geneutraliseerd.
Van klinische observatie tot genetische ontdekking
Het pad naar deze ontdekking was geen rechte lijn, maar het resultaat van twee complementaire onderzoeksbenaderingen die meer dan twee decennia overspannen.
** Dr. Thein ‘ s aanpak: de Families volgen*
Dr. Thein ‘ s werk begon met een bedrieglijk eenvoudige klinische vraag: * Waarom hebben sommige patiënten met bèta-thalassemie Opmerkelijk milde symptomen terwijl anderen levenslange transfusies nodig hebben?
Hij merkte op dat patiënten met mildere vormen van de ziekte vaak van nature hoge niveaus van foetaal hemoglobine bezaten. Om de genetische oorzaak te vinden, reisde Thein naar Malawi, waar hij een grote familie van meerdere generaties identificeerde met ongewoon milde gevallen van de ziekte. Door 210 individuen over zeven generaties te bestuderen, traceerde zijn team de eigenschap naar een specifiek genetisch gebied. Genome-brede associatie studies hebben uiteindelijk BCL11A aangewezen als de regulator die verantwoordelijk is voor deze variatie, wat bevestigt dat het een levensvatbaar therapeutisch doelwit is.
** Dr. Orkin ‘ s aanpak: Engineering the Cure**
Terwijl Thein het gen in menselijke populaties identificeerde, richtte Orkin zich op het bewijzen dat het therapeutisch kon worden gemanipuleerd. In 2011 ontwierp zijn team muizen met sikkelcelanemie en gebruikte genetische hulpmiddelen om het bcl11a-gen specifiek in hun zich ontwikkelende rode bloedcellen uit te schakelen. Het resultaat was opvallend: de muizen werden volledig gecorrigeerd en bleven gezond.
Dit proof-of-concept toonde aan dat het richten op één enkel gen voldoende was om de ziekte op te lossen. De komst van de CRISPR genbewerkingstechnologie leverde kort daarna het precieze hulpmiddel dat nodig was om dit muismodel te vertalen naar menselijke therapie.
Een nieuw tijdperk van behandeling
De theoretische doorbraak is nu klinische realiteit geworden. In 2023 werden de eerste genbewerkingstherapieën voor sikkelcelziekte goedgekeurd: Casgevy (door Vertex Pharmaceuticals en CRISPR Therapeutics) en Lyfgenia (door bluebird bio/Genetix Biotherapeutics).
De eerste resultaten van klinische proeven waren transformatief.
* * * Functionele genezing: * * meer dan 90% van de deelnemers aan de Vertex-studie vertoonde functionele verbetering.
* * * Symptoomresolutie: * * patiënten met sikkelcelziekte meldden een volledige beëindiging van pijnlijke crises.
* * * Transfusieonafhankelijkheid: * * patiënten met bèta-thalassemie hadden geen bloedtransfusies of beenmergtransplantaties meer nodig.
“Vroeger was het een ellendige ziekte… Nadat ze zijn behandeld, hebben ze een nieuw leven ingeblazen,” merkte Dr.Orkin op, die de diepgaande impact benadrukte op het vermogen van patiënten om normaal te werken en te leven.
De Toegankelijkheidsuitdaging
Ondanks de medische triomf blijven er aanzienlijke belemmeringen bestaan met betrekking tot de toegang. Huidige goedgekeurde therapieën zijn * * ex vivo * * behandelingen, wat betekent dat ze vereisen:
1. Het oogsten van de stamcellen van de patiënt.
2. Ze worden bewerkt in een gespecialiseerd laboratorium.
3. Het toedienen van intensieve chemotherapie om het beenmerg te verwijderen.
4. De bewerkte cellen opnieuw gebruiken.
Dit proces is fysiek uitputtend, logistiek complex en buitengewoon duur, kost tussen de 2 en 3 miljoen dollar per patiënt. Bijgevolg zijn deze behandelingen momenteel ontoegankelijk voor de populaties in Afrika ten zuiden van de Sahara en India die de hoogste last van de ziekte dragen.
The Road Ahead: Towards Simpler Cures
Door deze beperkingen te erkennen, draait de wetenschappelijke gemeenschap naar oplossingen van de volgende generatie. Zowel Dr. Thein als Dr. Orkin zijn nu gericht op * * kleine moleculetherapieën * * – geneesmiddelen die als een pil kunnen worden ingenomen in plaats van complexe genbewerking te vereisen.
-
-
- Orkin ‘ s Lab * * onderzoekt de gedetailleerde mechanismen van de hemoglobineschakelaar om geneesmiddelen te ontwikkelen die het lichaam farmacologisch kunnen terugbrengen naar het produceren van foetaal hemoglobine.
-
-
-
- Het onderzoek van Thein * * is gericht op kleine moleculen die ernstige pijncrises kunnen voorkomen of afbreken, waarbij een onmiddellijke en onvervulde klinische behoefte wordt aangepakt.
-
Hoewel de huidige gentherapieën een krachtige remedie bieden voor degenen die er toegang toe hebben, is het uiteindelijke doel om betaalbare, toegankelijke behandelingen te ontwikkelen die patiënten wereldwijd kunnen bereiken. De ontdekking van BCL11A heeft de kaart opgeleverd; de volgende stap is het bouwen van voertuigen die deze remedie naar elke hoek van de wereld kunnen brengen.
Conclusie
De identificatie van het bcl11a-gen vertegenwoordigt een monumentale sprong in de behandeling van sikkelcelziekte, van management naar functionele genezing. Hoewel de huidige gentherapieën duur en complex zijn, valideren ze het wetenschappelijke pad en drijven ze dringend onderzoek naar eenvoudiger, toegankelijker op geneesmiddelen gebaseerde behandelingen voor de miljoenen die nog steeds in nood zijn.