A doença falciforme tem sido uma condição hereditária devastadora, afetando desproporcionalmente as comunidades na África subsaariana e na Índia. Durante décadas, os pacientes suportaram ciclos de crises dolorosas excruciantes e exaustão severa, sem uma verdadeira cura à vista. Essa paisagem mudou drasticamente. Após anos de meticulosa pesquisa genética, os cientistas desbloquearam um mecanismo para curar funcionalmente a doença, enganando o corpo para produzir células sanguíneas saudáveis.
Em reconhecimento a esta descoberta transformadora, o Breakthrough Prize in Life Sciences concedeu 3 milhões de dólares ao Dr. Swee Lay Thein e ao Dr. Stuart Orkin. Seu trabalho identificou um “interruptor” genético específico que, quando invertido, permite que o corpo contorne os genes defeituosos responsáveis pela doença falciforme e beta-talassemia.
A Chave Biológica: Despertar A Hemoglobina Fetal
Para entender o avanço, é essencial observar como o sangue humano se desenvolve. No útero, os seres humanos produzem * * hemoglobina fetal, uma proteína altamente eficiente na extração de oxigênio da circulação da mãe. Logo após o nascimento, o corpo naturalmente interrompe essa produção e muda para hemoglobina adulta**.
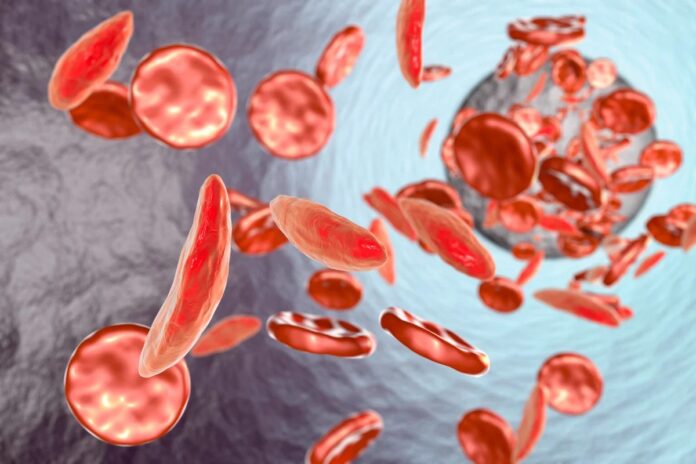
Em indivíduos com doença falciforme ou beta-talassemia, a hemoglobina adulta é malformada ou deficiente, levando às características hemácias em forma de foice que obstruem os vasos e causam dor. No entanto, a hemoglobina fetal permanece perfeitamente capaz de transportar oxigênio ao longo da vida. O único obstáculo era que os cientistas não sabiam como manter a linha de produção fetal funcionando após o nascimento.
A descoberta crítica foi a identificação de um gene chamado BCL11A. Este gene actua como um supressor, desligando activamente a produção de hemoglobina fetal à medida que crescemos. Orkin e Thein perceberam que, se pudessem desativar o BCL11A, poderiam persuadir o corpo a continuar a produzir hemoglobina fetal saudável, neutralizando efetivamente os efeitos da doença.
Da observação clínica à descoberta genética
O caminho para esta descoberta não foi uma linha recta, mas um resultado de duas abordagens de investigação complementares ao longo de duas décadas.
** Abordagem do Dr. Thein: seguir as famílias*
O trabalho do Dr. Thein começou com uma pergunta clínica enganosamente simples: * Por que alguns pacientes com beta-talassemia apresentam sintomas notavelmente leves, enquanto outros requerem transfusões ao longo da vida?
Ele notou que os pacientes com formas mais leves da doença geralmente possuíam níveis naturalmente altos de hemoglobina fetal. Para encontrar a causa genética, Thein viajou para o Malawi, onde identificou uma grande família multigeracional com casos invulgarmente ligeiros da doença. Ao estudar 210 indivíduos em sete gerações, sua equipe traçou a característica para uma região genética específica. Estudos de associação em todo o genoma eventualmente apontaram * * BCL11A * * como o regulador responsável por esta variação, confirmando-a como um alvo terapêutico viável.
** Abordagem do Dr. Orkin: Engenharia da cura**
Enquanto Thein identificou o gene em populações humanas, Orkin concentrou-se em provar que poderia ser manipulado terapeuticamente. Em 2011, sua equipe projetou camundongos com anemia falciforme e usou ferramentas genéticas para desativar o gene BCL11A especificamente em seus glóbulos vermelhos em desenvolvimento. O resultado foi surpreendente: os ratos foram completamente corrigidos e permaneceram saudáveis.
Esta prova de conceito demonstrou que visar um único gene era suficiente para resolver a doença. A chegada da tecnologia de edição genética CRISPR pouco depois forneceu a ferramenta precisa necessária para traduzir este modelo de ratinho em terapia humana.
Uma nova Era de tratamento
O avanço teórico tornou – se agora Realidade clínica. Em 2023, foram aprovadas as primeiras terapias de edição genética para a doença falciforme: Casgevy (pela Vertex Pharmaceuticals e CRISPR Therapeutics) e Lyfgenia (pela bluebird bio/Genetix Biotherapeutics).
Os primeiros resultados dos ensaios clínicos foram transformadores.
* * * Cura funcional: * * mais de 90% dos participantes no ensaio Vertex apresentaram melhoria funcional.
* * * Resolução dos sintomas: * * pacientes com doença falciforme relataram uma cessação completa das crises dolorosas.
* * * Independência Transfusional: * * os doentes com beta-talassemia deixaram de necessitar de transfusões de sangue ou de transplantes de medula óssea.
“Antes, era uma doença miserável… Depois de serem tratados, eles têm um novo sopro de vida”, observou o Dr. Orkin, destacando o profundo impacto na capacidade dos pacientes de trabalhar e viver normalmente.
O Desafio Da Acessibilidade
Apesar do Triunfo médico, subsistem barreiras significativas no que respeita ao acesso. As terapias actualmente aprovadas são tratamentos * * ex vivo**, o que significa que requerem:
1. Colheita das células estaminais do doente.
2. Editá – los em um laboratório especializado.
3. Administração de quimioterapia intensiva para limpar a medula óssea.
4. Reinfusão das células editadas.
Este processo é fisicamente extenuante, logisticamente complexo e extraordinariamente caro, custando entre $2 milhões e $3 milhões por paciente. Consequentemente, estes tratamentos são actualmente inacessíveis às populações da África subsariana e da Índia, que são as que mais sofrem da doença.
O Caminho A Seguir: Rumo A Curas Mais Simples
Reconhecendo estas limitações, a comunidade científica está a orientar-se para soluções de próxima geração. Tanto o Dr. Thein quanto o Dr. Orkin estão agora focados em * * terapias de pequenas moléculas— * – drogas que podem ser tomadas como uma pílula em vez de exigir edição genética complexa.
-
-
- O Laboratório de Orkin * * está investigando os mecanismos detalhados da mudança da hemoglobina para desenvolver drogas que podem reverter farmacologicamente o corpo para produzir hemoglobina fetal.
-
-
-
- A investigação de Thein * * centra-se em pequenas moléculas que podem prevenir ou abortar crises graves de dor, abordando uma necessidade clínica imediata e não satisfeita.
-
Embora as terapias genéticas atuais ofereçam uma cura poderosa para aqueles que podem acessá-las, o objetivo final é desenvolver tratamentos acessíveis e acessíveis que possam chegar aos pacientes em todo o mundo. A descoberta do BCL11A forneceu o mapa; o próximo passo é construir veículos que possam levar essa cura a todos os cantos do mundo.
** Conclusão**
A identificação do gene BCL11A representa um salto monumental no tratamento da doença falciforme, passando do manejo para a cura funcional. Embora as terapias genéticas atuais sejam caras e complexas, elas validam o caminho científico, conduzindo pesquisas urgentes em direção a tratamentos baseados em medicamentos mais simples e acessíveis para os milhões que ainda precisam.